遺伝子:生体膜干渉
~生体膜干渉~
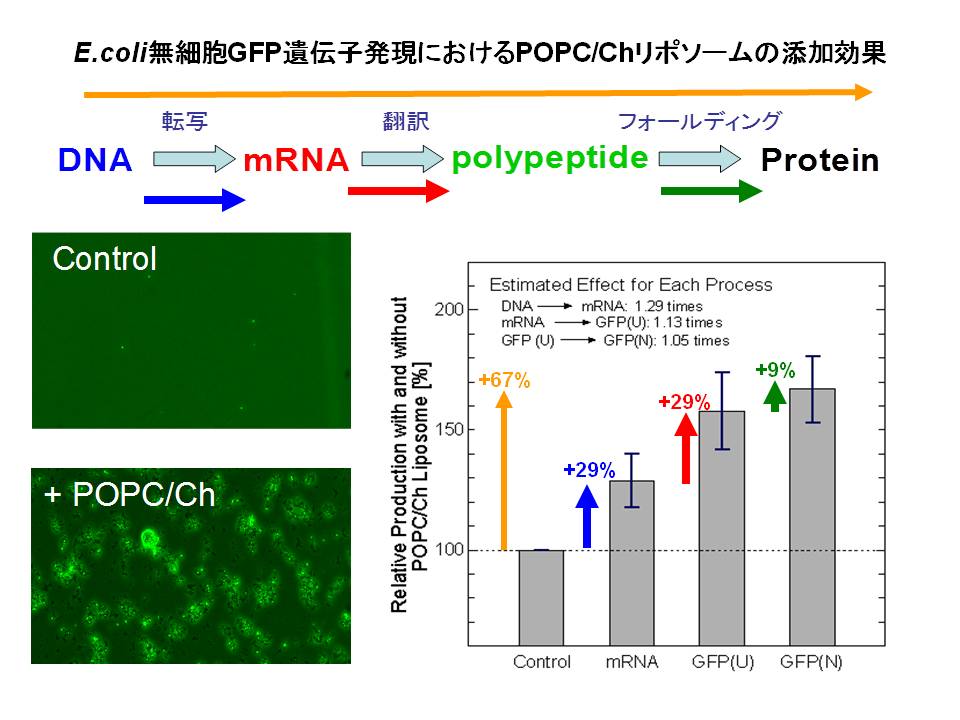
細胞内(~20μm)では遺伝子(DNA)からRNAを経てタンパク質が効率よくつくられています.遺伝子発現は様々な生体分子(DNA,mRNA,ポリペプチド(unfold),RNAポリメラーゼ,ribosome,tRNA,各種基質,他)を必要とします.従来では,細胞膜のような脂質膜はただの格納容器として考えられてきましたが,私たちは,モデル生体膜あるリポソーム膜表面で,無細胞GFP発現系が素過程レベル(転写,翻訳,フォールディング)で制御されることを明らかにしました(Fig. 1).リポソームの表面特性(表面電荷密度,膜流動性,ドメイン性)に着目して素過程におけるリポソーム添加効果を解析したところ,特にリポソームはRNA分子と相互作用しやすい事が分かりました.リポソーム膜表層をデザインすることによりmRNA翻訳を0~150%まで制御することに成功しています(⇔RNAi).本研究結果より,リポソームが無細胞遺伝子発現系に“干渉”することを世界に先駆けて明らかにしました(“生体膜干渉”).
Fig. 1 リポソームによる遺伝子発現素過程の制御
~RNA分子の識別分離を目標とするリポソーム表層デザイン~
リポソームの表面特性に応じてRNA分子の親和性が影響されることが明らかとなっています(Fig. 2).たとえば,水素結合ドナー/アクセプタを有するコレステロール(Chol)をリポソームに修飾した場合,Cholがクラスタを形成し,さらに相互作用が集積化されることでより強い相互作用が誘導されました.すなわち,制御の“鍵”はリポソーム表層のミクロ膜特性(ミクロ相分離,ナノドメイン形成)です.RNA分子を構成する核酸塩基(A, U, G, C)やRNA高次構造(A-formヘリックス)にマッチするリポソーム膜表層をデザインすることによる,高度な“識別分離”を目指して研究を行っています.
Fig. 2 RNA分子の識別分離を目標とするリポソーム膜表層デザイン
~研究の展開~
リポソーム膜表層を最適にデザインすることでRNA分子との相互作用だけでなく,RNA分子の高次構造やRNA機能を制御できることも明らかになっています.制御対象であるRNA分子のバリエーションを拡大し,RNA分子の機能制御のためのリポソーム膜表層デザインについても研究を進めています.
・Hammerhead ribozymeの高次構造形成による自己切断反応制御
・過酸化水素による膜構造変化をトリガーとするmRNA再活性化(Off→On制御)
・正電荷ドメイン性リポソームによる活性化mRNA-リポソーム複合体の形成
このようにリポソーム膜を機能性材料として,DDSやRNA創薬,Origin of Life等,様々な研究展開が期待されます.
Fig. 3 リポソーム膜を基盤とするRNA機能制御への展開
[関連する論文]
- Huong Thi Bui, Hiroshi Umakoshi, Kien Xuan Ngo, Masato Nishida, Toshinori Shimanouchi, Ryoichi Kuboi,
Liposome membrane itself can affect gene expression in the Escherichia coli cell-free translation system,
Langmuir 24 (19), pp. 10537-10542 (2008) - Hiroshi Umakoshi, Masato Nishida, Keishi Suga, Huong Thi Bui, Toshinori Shimanouchi, Ryoichi Kuboi,
Characterization of Green Fluorescent Protein Using Aqueous Two-Phase Systems,
Solv. Extr. Res. Dev. Japan, 16, pp. 145-150 (2009) - Huong Thi Bui, Hiroshi Umakoshi, Keishi Suga, Masato Nishida, Toshinori Shimanouchi, Ryoichi Kuboi,
Negatively Charged Liposome as a Potent Inhibitor of Post-Translation during in vitro Synthesis of Green Fluorescent Protein,
Biochem. Eng. J., 46 (2), pp. 154-160 (2009) - Huong Thi Bui, Hiroshi Umakoshi, Keishi Suga, Tomoyuki Tanabe, Toshinori Shimanouchi, Ryoichi Kuboi,
Cationic Liposome Inhibits Gene Expression in an E. coli Cell-Free Translation System,
Membrane, 34 (3), pp. 146-151 (2009) - Hirhoshi Umakoshi, Keishi Suga, Huong Thi Bui, Masato Nishida, Toshinori Shimanouchi, Ryoichi Kuboi,
Charged Liposome Affects the Translation and Folding Steps of in vitro Expression of Green Fluorescent Protein,
J. Biosci. Bioeng., 108 (5), pp. 450-454 (2009) - Keishi Suga, Hiroshi Umakoshi, Hibiki Tomita, Tomoyuki Tanabe, Toshinori Shimanouchi, Ryoichi Kuboi,
Liposomes Destabilize tRNA during Heat Stress,
Biotechnol. J., 5 (5), pp. 526-529 (2010) - Huong Thi Bui, Hiroshi Umakoshi, Keishi Suga, Tomoyuki Tanabe, Kien Xuan Ngo, Toshinori Shimanouchi, Ryoichi Kuboi,
Cationic Liposome can Interfere mRNA Translation in an E. coli Cell-Free Translation System,
Biochem. Eng. J., 52 (1), pp. 38-43 (2010) - Hiroshi Umakoshi, Tomoyuki Tanabe, Keishi Suga, Huong Thi Bui, Toshinori Shimanouchi, Ryoichi Kuboi,
Oxidative Stress can Affect the Gene Silencing Effect of DOTAP Liposome in an in vitro Translation System,
Int’l. J. Biol. Sci., 7 (3), pp. 253-260 (2011) - Keishi Suga, Tomoyuki Tanabe, Hibiki Tomita, Toshinori Shimanouchi, Hiroshi Umakoshi,
Conformational Change of Single-Stranded RNAs Induced by Liposome Binding,
Nucl. Acids Res., 39 (20), pp. 8891-8900 (2011) - Keishi Suga, Hibiki Tomita, Seishiro Tanaka, Hiroshi Umakoshi,
Hydrophobic Properties of tRNA with Varied Conformations Evaluated by an Aqueous Two-Phase System,
Int’l. J. Biol. Sci., 8 (8), 1188-1196 (2012) - Keishi Suga, Tomoyuki Tanabe, Hiroshi Umakoshi,
Heterogeneity of the Cationic Liposome Membrane Can Regulate mRNA Conformation and the in vitro Gene Translation in the Cell-free System,
Langmuir, submitted - Keishi Suga, Hiroshi Umakoshi,
Characterization of Nano-Sized Ordered Domain in DOPC/DPPC Binary Liposome by TEMPO Quenching Method,
to be submitted - Keishi Suga, Seishiro Tanaka, Hiroshi Umakoshi,
Liposome Can Affect the Self-Cleavage Reaction of Hammerhead Ribozyme without Mg2+,
in preparation